肠道微生物与脑-肠轴交互作用的研究进展丨微生态前沿
自19世纪末美国学者率先提出肠脑概念,胃肠道与中枢神经间存在双向沟通机制逐渐被揭开,众多参与大脑功能调节的神经肽与神经递质如多巴胺、5-羟色胺、一氧化碳、去甲肾上腺素等相继在肠道中被发现,由免疫、神经通路与内分泌途径共同参与构成的脑-肠轴通路在调控肠道功能与维持宿主健康方面发挥着重要作用。近十年来,大量的动物和临床前研究表明肠道菌群不仅参与调节宿主代谢及免疫等生理过程,同时广泛参与脑-肠轴通路,在胃肠道与中枢神经系统双向应答中扮演重要角色。微生物-胃肠-脑轴正逐步取代脑-肠轴在神经系统疾病预防与治疗方面发挥更精准的调节作用。
前期研究表明,大脑可通过中枢神经系统调节微生物的组成与行为,但同时肠道微生物也可借助包括内分泌系统、免疫系统、神经内分泌及代谢系统在内的多种通路参与对大脑信号的调节,触发微生物-胃肠-脑轴双向应答机制。
肠神经系统由胃肠道壁内神经成分组成,具有调节控制胃肠道的功能,被称为“第二大脑”。它与中枢神经系统间的沟通主要经由迷走神经介导,因此,迷走神经在肠道微生物群影响脑-肠轴功能中发挥重要作用。肠神经系统通过与迷走神经形成突触连接,组成“肠道菌群-肠神经-迷走神经-脑”信息传递途径。
德国最新研究发现,用抗生素杀伤肠道菌群会影响大脑海马体的神经功能,并揭示了Ly6Chi白细胞在参与大脑、免疫系统与肠道通讯中发挥至关重要作用。美国一项相关研究发现,益生菌对大脑异常行为的改善作用由迷走神经介导,摄入乳酸菌可改善小鼠焦虑情绪,伴随大脑γ-氨基丁酸受体的表达升高。而在切断迷走神经后,改善性作用减弱甚至消失。
肠道微生物一方面通过调节肠道内分泌细胞分泌脑肠肽、促肾上腺皮质激素释放因子、肾上腺皮质酮等激素类物质直接作用于脑,另一方面也可借助胃泌素、胰多肽、促胰酶肽、瘦素等肠多肽类分泌调节宿主摄食、能量平衡及生理节律等多种生理行为。胃肠道内寄居的大量微生物通过合成的生长抑素、乙酰胆碱或孕酮等内分泌激素,主动识别宿主的同源受体,一旦肠道内外相应激素达到一定水平即可改变宿主的神经电生理过程。
肠道微生物直接激活迷走神经影响免疫系统功能,启动与中枢神经系统间的双向沟通。另外,胃肠菌群在先天免疫方面通过改变体循环中促炎性/抗炎性因子水平间接影响大脑功能。研究表明外周血中CRP、IL-1、IL-6、TNF等炎症标记物升高均可影响大脑功能导致抑郁。
肠道微生物代谢产物会对脑-肠轴及机体免疫系统产生调节作用。以短链脂肪酸为例,它是细菌对外源食物中碳水化合物发酵而产生,可通过多种通路参与脑-肠轴间调节活动。首先,短链脂肪酸通过G蛋白偶联受体GPR41及GPR43刺激交感神经及自主神经系统;其次,短链脂肪酸通过调节血脑屏障通透性,维持中枢神经系统内环境稳定,影响大脑发育及行为,该机制被证实参与自闭症的发生发展。不仅如此,短链脂肪酸同样参与神经胶质细胞的稳态调节,在维持脑部发育及脑组织自稳态中发挥重要作用。
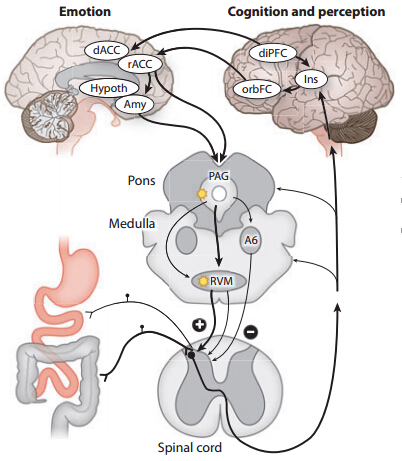
目前已知包括肠易激综合征(IBS)在内的相关功能性肠病的发生往往受到脑-肠轴调节功能失衡的影响。现今更多的研究结果揭示微生物-胃肠-脑轴调节功能改变很可能作为一种潜在的脑功能失调的病理生理机制参与自闭症、帕金森病、情绪行为失控及慢性疼痛等中枢神经系统疾病的发生发展。
肠道微生态构成不仅与胃肠疾病发生相关,同时也会对应激性神经反应产生影响。Marshall在一项为期8年的研究中发现,IBS患者存在抑郁症和焦虑症的风险更高。此外,De Palma等发现,将IBS患者排泄物中的微生物植入小鼠体内后,这些小鼠同样表现出了焦虑行为;相反,把健康人肠道内的微生物植入小鼠体内后,则没有这种反应。
自闭症也称为孤独症,涉及一系列复杂的神经发育障碍。前期研究表明肠道微生物的发育和儿童脑发育过程是同步的,自闭症发病阶段与肠道菌群的发育过程的时间节点具有相似性。目前的研究发现,自闭症患者肠道中的梭菌属、普氏菌属、脱硫弧菌属及白色念球菌属与正常对照组存在差异,并且厚壁菌门与拟杆菌门的比值也显著区别于正常对照组。
PD早期多出现胃肠道功能失调症状,起始病变为肠神经系统损伤,是一种经迷走神经逐步向中枢神经系统进展的慢性神经退行性疾病。大量研究表明肠道菌群紊乱与PD间存在密切关系,肠道微生物改变可能早于PD发生。有学者认为肠道微生物群的变化可引起肠道炎症反应,从而触发α-突触核蛋白(α-SYN)的错误折叠,α-SYN的非正常聚积是PD的典型病理特点。同时也有研究认为,PD患者中存在结肠炎症,可增强外周炎症反应促进PD进展。相应研究提示肠道菌群改变常会造成PD症状改变,感染幽门螺旋杆菌人群更易患PD,而给PD患者服用根除幽门螺旋杆菌的抗生素药物可以显著改善患者的PD症状。
肠道微生物菌群稳定组成是发挥微生物-胃肠-脑轴双向调控的基础。不合理饮食、抗生素使用、饮酒、吸烟以及昼夜节律失调等外界因素会影响微生物组成,在破坏人体微生态稳定的同时直接影响胃肠-中枢神经系统平衡的精确调控,尤以饮食因素影响最大。
Bercik等认为饮食作为影响肠道菌群组成及功能的关键核心,参与微生物-胃肠-脑轴各项调节通路,调控大脑与神经系统功能发挥。大量研究表明,高脂饮食可以显著改变肠道菌群多样性并降低突触可塑性,增加易损性,引起小鼠焦虑行为。与之相比,给予幼鼠低热量饮食会促进神经形成,增加脑源性神经生长因子分泌,改善其成年阶段的认知能力。
在微生态稳定调控方面,益生菌、益生元及合生元被认为可调节胃肠-脑轴双向作用,能有效影响大脑活性与行为。动物及临床研究表明益生菌与益生元制剂可发挥间接作用,增加肠道有益菌数量,改善肠道菌群结构,在保护胃肠粘膜屏障完整性的同时发挥免疫调节作用,能有效调节肠道菌群失衡引起的各类胃肠道疾病与精神疾病。
参考文献 田祖宏《肠道微生物与脑- 肠轴交互作用的研究进展》



